

异基因造血干细胞移植是治疗白血病、淋巴瘤、再生障碍性贫血等重症血液疾病的重要手段,而急性移植物抗宿主病(Acute Graft-Versus-Host Disease,aGVHD) 是移植后早期最常见、最危险的并发症,也是影响移植成功率的关键因素。
急性GVHD通常发生在移植后100天以内,简单来说,就是供者的免疫细胞“不认”受者身体,把受者的正常组织当成敌人发起攻击,造成皮肤、肠道、肝脏等多器官严重损伤,严重时可导致器官衰竭甚至死亡。
正常情况下,人体免疫系统能区分“自身”和“外来”物质,避免攻击自身组织。但在异基因移植中,供者干细胞里的成熟T淋巴细胞进入受者体内后,会识别出受者细胞表面的人类白细胞抗原(HLA)或组织相容性抗原存在差异,将其判定为“异物”,进而启动强烈的免疫反应,最终引发全身炎症与组织破坏。
急性GVHD的发病机制是一个多阶段、级联放大的免疫过程,经典理论将其概括为“三步致病模型”。
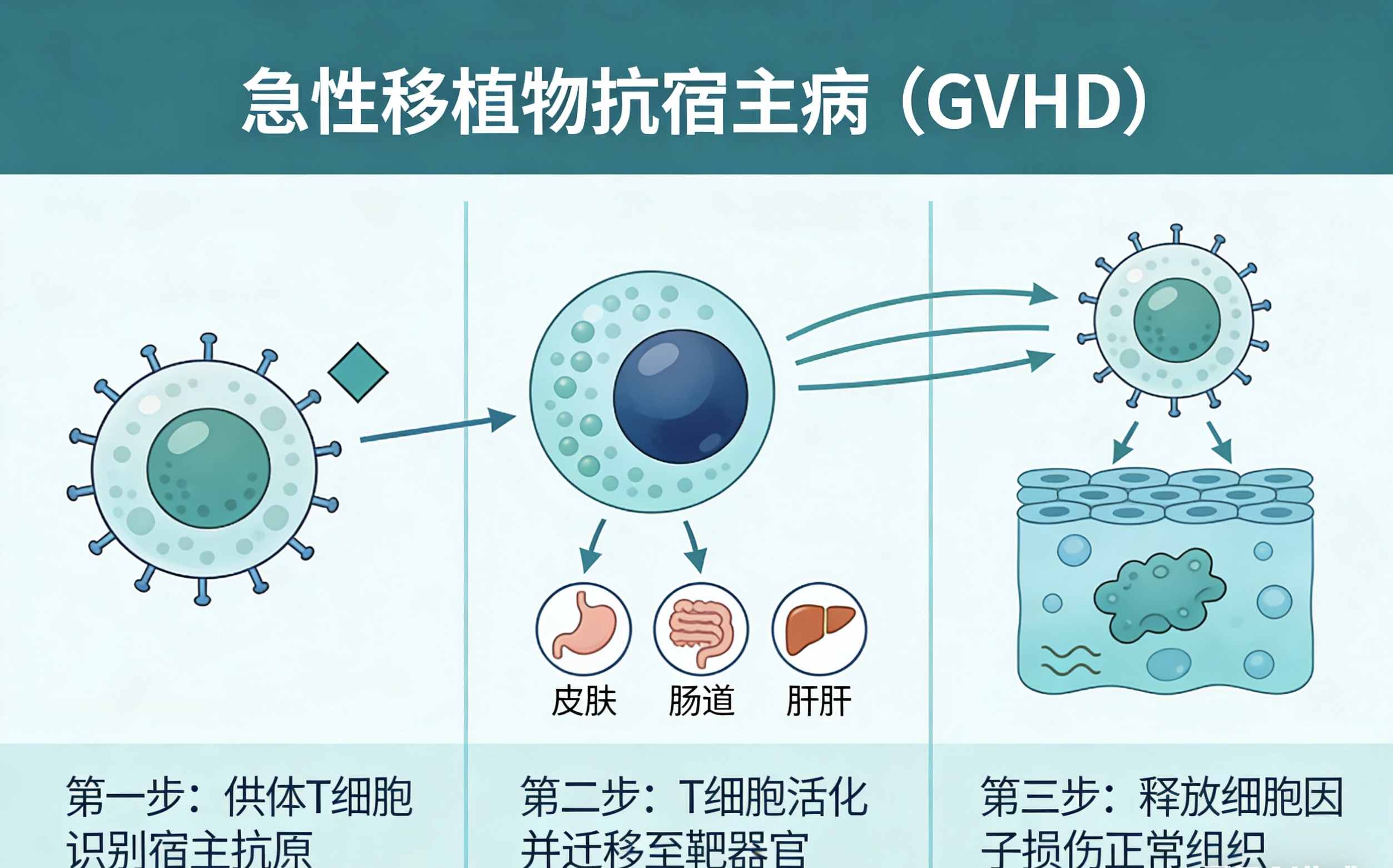
第一步,预处理造成组织损伤,启动炎症环境。移植前患者需接受化疗或放疗,目的是清除肿瘤细胞、抑制自身免疫、为供者干细胞腾出生长空间。但这一过程会直接损伤肠道黏膜、皮肤屏障等正常组织,导致大量损伤相关分子释放,激活受者体内的抗原呈递细胞,同时引发全身性轻度炎症,为后续免疫反应做好“铺垫”。
第二步,供者T细胞识别、活化与增殖。供者T细胞是引发GVHD的核心效应细胞。它们通过识别供受者间的HLA差异或次要组织相容性抗原,被充分激活并大量增殖、分化为效应T细胞。这一步是急性GVHD发生的核心环节,HLA配型越不匹配,反应往往越剧烈。
第三步,细胞因子风暴与靶器官损伤。活化的免疫细胞释放肿瘤坏死因子、白细胞介素等多种炎性因子,形成“细胞因子风暴”,进一步招募更多免疫细胞聚集,放大炎症反应。这些免疫细胞和炎症因子集中攻击皮肤、胃肠道、肝脏三大靶器官,导致典型临床表现:皮肤出现红斑、皮疹甚至剥脱性皮炎;肠道表现为恶心、呕吐、腹泻、血便;肝脏则出现黄疸、肝功能异常。
除经典三步机制外,先天免疫激活、肠道菌群紊乱、黏膜屏障破坏等也会加重病情。临床上根据受累器官及严重程度分级,轻者仅轻微皮疹,重者可快速进展为多器官衰竭。
目前急性GVHD以预防为主,移植后常规使用免疫抑制剂降低风险。一旦发病,需根据分级及时使用激素、靶向药物等控制免疫攻击。
总而言之,急性GVHD本质是供者免疫细胞对受者组织的过度免疫攻击,是移植后免疫系统重建过程中的“失控内战”。深入理解其发病机制,有助于更精准地预防和治疗,从而提高移植患者的长期生存率与生活质量。
 0
0


